
当前mRNA-LNP新冠疫苗的一个缺点是它们必须在(超)低温下储存,了解这些疫苗不稳性的根本有助于合理提高mRNA-LNP产品的稳定性,从而降低对储存温度的要求。
一篇发表于International Journal of Pharmaceutics2021年5月刊的题为“mRNA-lipid nanoparticle COVID-19 vaccines: Structure and stability”的文章对这一话题的关键要素进行了分析讨论。这篇综述讨论了mRNA-LNP可能的内部结构、影响mRNA-LNP稳定性的因素以及优化mRNA-LNP产品稳定性的策略。下文将截取其中部分内容。

导致mRNA疫苗体外不稳定的因素
对mRNA-LNP结构的分析表明,mRNA、可电离的阳离子脂质和水存在于LNP核心中,中性辅助脂质主要位于包裹的外壁。mRNA水解是mRNA-LNP不稳定的主要因素。
为了提高mRNA-LNP疫苗的稳定性,首先,应优化mRNA的核苷酸组成。其次,更好地了解mRNA在LNP核心中所处的环境可能有助于合理调整LNP结构以保持mRNA的完整性。此外,干燥技术如冻干,可能是仍有待探索的可行途径。
mRNA体外稳定性的分析方法
文献中表示,下列分析评价方法汇总表来自Poveda等人的综述。
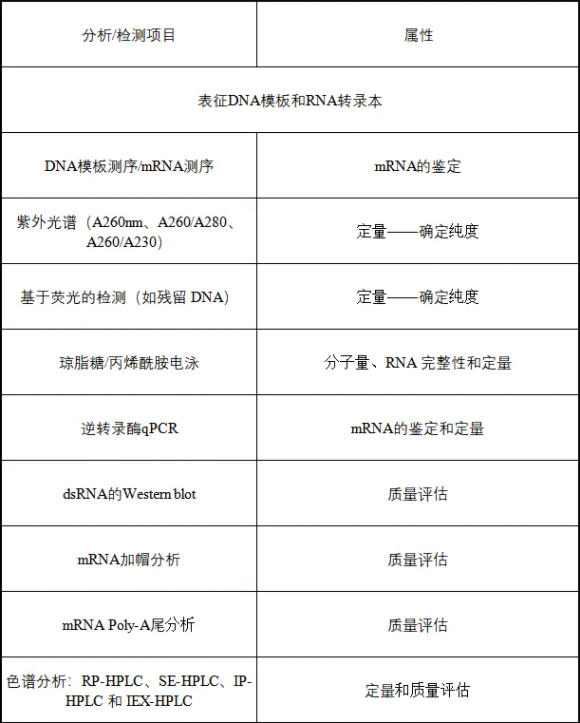
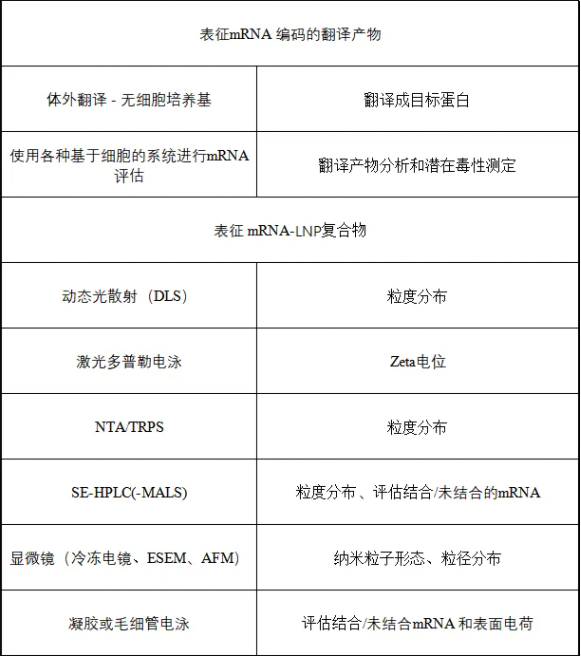
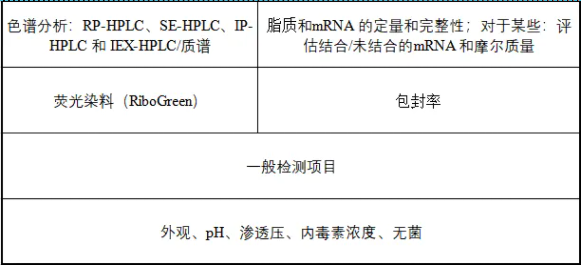
其中部分检测方法旨在直接检测裸露的mRNA结构,因此对于这些稳定性检测方法,包装在递送系统中的mRNA疫苗需先从LNP中释放出mRNA,其释放程度需控制以降低潜在的包装影响。
凝胶电泳:可提供mRNA大小和完整性的信息。目前已有商用电泳设备用于mRNA的高通量分析。若检测到mRNA长度处的条带强度降低、条带变宽或者出现新的条带,则提示mRNA链变短,可能存在降解并发生链断裂。
荧光相关光谱(FCS):可用于检测mRNA大小的变化,主要原理是通过荧光标记的mRNA 的布朗运动来计算分子量。然而,这种技术需要荧光标记,与凝胶电泳相比准确度并不一定更高,并且只能检测到包括分子量发生显著变化的mRNA 降解,例如链断裂等。
高效液相色谱仪(HPLC):各类高效液相色谱仪中,已有一些专利和文献证实RP-HPLC、SE-HPLC、IP-HPLC 和 IEX-HPLC 方法能够成功应用于大分子mRNA纯度和稳定性的分析。其中一些技术也可用于mRNA 制备纯化。
IEX-HPLC可用于测量游离和LNP 包封的 mRNA。上表中提到的荧光染料(RiboGreen)技术可以建立相同参数的正交技术,然而使用相同的mRNA-LNP样品却测定出了不同的含量结果;与RiboGreen数据相比,IEX-HPLC 结果与体内数据的相关性更好。这说明即使是像 RiboGreen检测这样的成熟技术,也应该根据具体情况进行详细验证。
RT-qPCR:可用于分析mRNA降解。可测定能转录成完整目标cDNA的mRNA 总量,这表明所有影响这个过程的因素都可以间接定量检测。RT-qPCR技术的另一个优点是能定量检测影响转录的所有类型的降解,而之前讨论的其它技术只能检测mRNA 的大小。
然而,RT-qPCR 技术也有一定的局限性,由于所用酶存在错误率,导致结果有时不太可靠。而且RT-qPCR 技术这目前没有被广泛使用,并且无法区分不同类型的降解。
荧光信号测量:使用编码荧光蛋白的mRNA,可以通过测量荧光信号间接确定mRNA的完整性,该方法依赖于体外实验中mRNA在细胞内的表达。这种方法有助于为生物活性 mRNA-LNP 设计和处方筛选研究提供指导。
酶联免疫吸附试验 (ELISA)/蛋白质印迹技术(WB):可用于确定编码非荧光抗原的mRNA 的翻译功效。其优点在于,它给出了制剂的整体完整性和可能影响 mRNA 转录的所有因素的总和。其局限性在于,检测结果精确性较低,无法明确mRNA破坏的类型,且时间成本较高。
本文来源自:医麦克微信公众号,本文仅作信息交流之目的,如侵权请联系删除。